肺高血圧症の病態の解明、診断能と治療成績の向上、および治療指針の確立をはかり、貢献することを目的として活動を行っております
本学会について
2025年度 日本肺高血圧・肺循環学会「学会奨励賞」基礎研究賞 受賞者
2025年度「学会奨励賞」基礎研究賞 受賞者および受賞研究題目(五十音順)
藤原 隆行(東京大学医学部附属病院コンピュータ画像診断学・予防医学講座/循環器内科)
「三次元病理病態解析システムを用いた低酸素誘導性肺高血圧モデルにおける代償的血管新生の発見およびその治療応用」
研究要旨
肺動脈性肺高血圧症(Pulmonary arterial hypertension: PAH)は、肺動脈の狭窄により肺血管抵抗の上昇・右心不全を引き起こす予後不良の難治疾患である。現在のPAH治療薬は血管拡張作用を主体とするが、PAH病態進展の根本に作用するものではないため、新たな機序による治療薬開発が喫緊の課題である。PAHの血管リモデリングとしては、血管内皮細胞および平滑筋細胞の異常増殖が知られているが、その一方で血管新生の関与も過去には報告されてきた。
PAHの最重症病変である叢状病変(plexiform lesion)において血管内皮成長因子(Vasular endothelial growth factor: VEGF)の発現が亢進していることより血管内皮細胞・平滑筋細胞の異常増殖へのVEGFの関与が示唆され、また低酸素誘導性肺高血圧症(PH)動物モデルにおいてVEGFの上流に位置する低酸素誘導因子(Hypoxia induced factor: HIF)の抑制によりPHが改善するなど、VEGFならびに血管新生がPHを増悪する方向であると考えられていた。その一方で、VEGF阻害薬であるSU5416を低酸素誘導性PH動物モデルに投与したところ、当初の予想とは反してPHは増悪し、また肺においてVEGFの発現を増強させることにより低酸素誘導ラットPHモデルが改善するなど、PHにおけるVEGFおよび血管新生の役割については混沌としている状況であった。
このPHにおけるVEGFおよび血管新生に関する理解が乏しい理由として、従来の二次元病理組織による形態評価では、枝分かれ構造などの複雑な血管形態の正確な描出は不可能であり、血管新生が生じているかそのものの判断が困難であることが原因ではないかと申請者は考えた。この障壁を克服すべく、組織透明化技術CUBIC(Tainaka K, et al. Cell.2014;159:911-924)および多光子顕微鏡を用いて、マウス組織全体全層の血管構造を三次元可視化するシステムの構築し、PHマウスモデルにおけるVEGFならびに血管新生の意義について解明することを目指した。
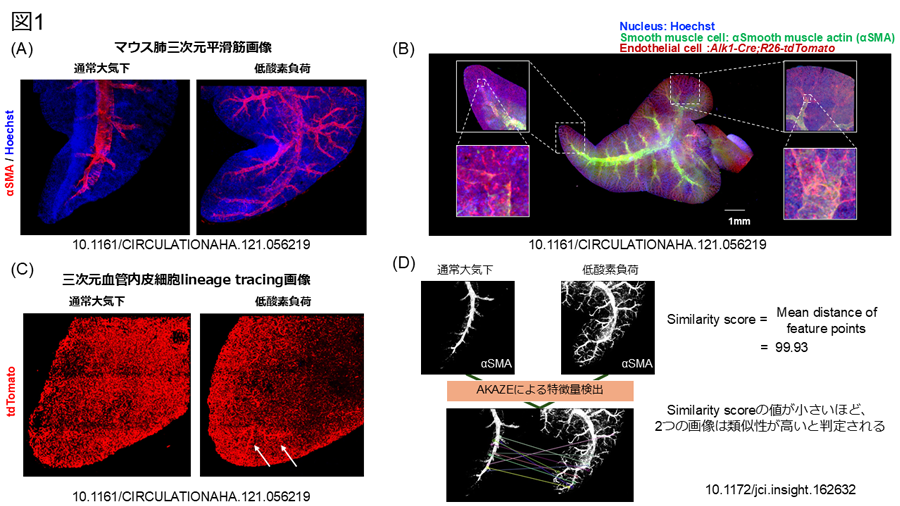
CUBICによりマウス肺組織は透明となり、抗αSMA-cy3抗体により平滑筋の染色は可能であった(図1A)。しかしながら血管内皮細胞については抗CD31抗体、抗CD102抗体、糖鎖抗体IsolectinB4などの染色を試みるもいずれも失敗に終わった。そこで蛍光レポーター蛋白を用いる方針とし、肺内皮細胞特異的にCreタンパクを発現するTg(Alk1-cre)-L1マウスにRosa26-CAG-lsl-tdTomatoマウスを掛け合わせて、肺内皮細胞特異的に蛍光タンパクtdTomatoを発現するマウスを作成したところ、血管内皮細胞の描出に成功し、両者を同時に描出することにより、一細胞解像度でマウス肺葉全体の血管描出に成功した(図1B、Fujiwara T, Circulation.2021;144:1452-1455.)。またより血管新生像を鋭敏に描出すべく、血管内皮細胞特異的にタモキシフェン誘導下にCreタンパクを発現するTg(Cdh5-cre/ERT2)マウスとRosa26-CAG-lsl-tdTomatoマウスを掛け合わせて、血管内皮細胞の三次元lineage tracingシステムの構築に成功した(図1C、Fujiwara T, Circulation.2021;144:1452-1455.)
さらには、従来三次元画像の解析においては、断層撮影された数多くの二次元画像を処理する必要があるためマシンパワーが必要であるにも関わらず、体積・表面積・距離などの計測にとどまっていた。申請者はこれらの指標では複雑な血管の三次元構造を評価するのに不十分であると考え、画像認識の手法である特徴量検出の一つ、AKAZEを用いて画像の類似性の評価を行うことを考案した。かつAKAZEは通常二次元画像のみ取り扱うため、三次元再構成により得られたMIP(Maximum Intensity Projection)画像もしくはVR(Volume Rendering)画像を用いることにより(2.5次元解析)取り扱うデータ量も大幅に削減することに成功した(図1D、Fujiwara T, JCI Insight. 2023;8:e162632.)。
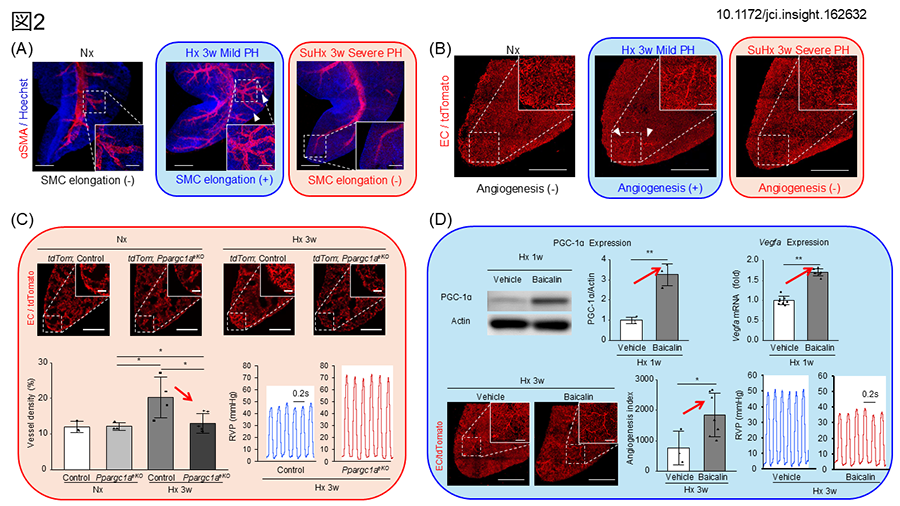
このマウス肺三次元病理病態解析システムを用いて、低酸素誘導性(Hx)PHマウスおよび低酸素誘導+SU5416(VEGF阻害薬)投与(SuHx)PHマウスの血管リモデリングの評価を行った。Hx-PHマウスにおいては、血管平滑筋細胞(図2A、Fujiwara T, JCI Insight. 2023;8:e162632.)、血管内皮細胞(図2B、Fujiwara T, JCI Insight. 2023;8:e162632.)ともに肺末梢への伸長を認め、血管新生が生じていると考えられたが、SuHx-PHマウスにおいてはその両者は認めず、さらにPHが増悪した。これらの結果から、マウスHx-PHにおいて血管新生は代償的な働きを担っていることが示唆された。この血管新生反応を制御する因子を探索したところ、低酸素負荷早期におけるVegfaの発現パターンおよび、HIFとは独立した血管新生制御因子であるPGC-1α(遺伝子名Ppargc1a)の発現パターンが、各PHモデルマウスの血管新生反応と類似していた。またPGC-1αの発現変化は特に肺内皮細胞に見られることを発見した。そこでHx-PHにおける肺内皮細胞PGC-1αの役割を検証すべく、肺内皮細胞特異的PGC-1αノックアウトマウス(Tg(Alk1-cre)-L1; Ppargc1afl/flマウス)を作成し、低酸素負荷を行ったところ、Vegfaの発現ならびに血管新生反応は減弱し、PHは増悪した(図2C、Fujiwara T, JCI Insight. 2023;8:e162632.)。その一方で内皮細胞においてPGC-1αの発現を上昇させる効果を持つフラボノイドの一種であるBaicalinをHx-PHに投与したところ、PGC-1αおよびVegfaの発現はさらに増強し、血管新生反応を促進するとともにPHは改善した(図2D、Fujiwara T, JCI Insight. 2023;8:e162632.)。以上の結果よりHIFとは独立した血管新生因子であるPGC-1αが、PHの新規治療標的として示唆された(Fujiwara T, JCI Insight. 2023;8:e162632.、Fujiwara T. Int Heart J. 2025;66:3-12.)。
2025年度 日本肺高血圧・肺循環学会「学会奨励賞」臨床研究賞 受賞者
2025年度「学会奨励賞」臨床研究賞 受賞者および受賞研究題目(五十音順)
桃井 瑞生(慶應義塾大学医学部循環器内科)
「クローン性造血に着目した慢性血栓塞栓性肺高血圧症の遺伝学的解析」
研究要旨
申請者は肺高血圧症における遺伝学的解析を主なテーマとして研究を行ってきた。これまで肺高血圧症領域では、肺動脈性肺高血圧症での遺伝学的研究が盛んに行われてきた一方、慢性血栓塞栓性肺高血圧症(以下CTEPH)では明確な家族性発症の症例が乏しいこともあり、遺伝学的研究が十分に進められてこなかった。申請者は、血液細胞での後天的な遺伝子の体細胞変異であるクローン性造血(Clonal hematopoiesis)に着目し、200人を超えるCTEPH患者で解析を行い、クローン性造血が血栓形成傾向や治療抵抗性と関連していること、好中球細胞外トラップ(以下NET)が血栓形成傾向に寄与していることを報告した(Momoi M, et al. J Am Heart Assoc. 2024;13:e035498.)。更に、申請者は末梢性肺動脈狭窄症(以下PPS)などの血管疾患の関連遺伝子として報告されているRNF213 p.R4810Kヘテロ接合性変異がCTEPH患者で6.4%に存在し、この変異を有する場合BPAへの反応が不良であることを報告した(Momoi M, et al. JACC: Asia. 2024;4:1017–1019.)。これらの研究により、申請者はCTEPH患者においても遺伝学的検査が病態生理や治療反応を予測する上で重要であることを示した。以下に研究の概要を記載する。
①CTEPHにおけるクローン性造血の意義
背景
CTEPHでは、一部の血栓素因が発症のリスクであるとされるが、血栓素因を持たない患者も多く、CTEPHを発症する原因の多くは未だ解明されていない。近年、造血幹細胞での体細胞変異であるクローン性造血が多くの心血管疾患と関連していることが報告されている。本研究では、CTEPH患者におけるクローン性造血の頻度や臨床的意義を検証した。
方法
CTEPH患者214人の血液検体からDNAを抽出し、全エクソームシーケンスおよびパネルシーケンスによる遺伝学的解析を行った。クローン性造血と関連した遺伝子変異を検出し、CTEPH患者においてクローン性造血を有している患者の頻度を確認した。クローン性造血による臨床的影響を評価するために、診断時の患者背景や治療前後の血行動態等を、クローン性造血を有する患者と有しない患者で比較した。また、患者の末梢血からRNAと血清を抽出し、RNAシーケンス解析及びタンパク質の定量分析を行った。
結果と考察
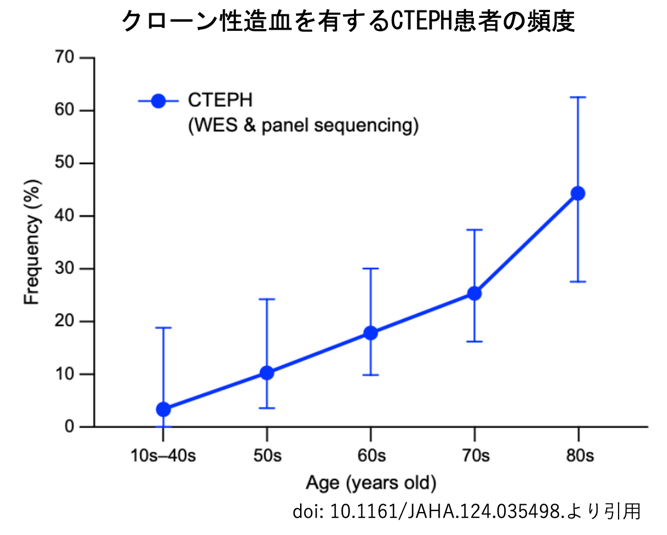 クローン性造血に関連した遺伝子変異を全体の20.1%のCTEPH患者で認めた。中でも年齢が80代の患者では、その割合は44.4%と非常に高かった。臨床的影響としては、クローン性造血を有するCTEPH患者では、治療1年後のBNPや在宅酸素療法使用率が高く、6分間歩行距離が短かった。また、クローン性造血を有する患者では、抗凝固療法を行っているにも関わらず、診断後肺動脈に新規血栓が出現するイベントの発生率が高く、さらには、治療完了後に病状が増悪し追加のBPA治療が必要となる頻度も高かった。これらの臨床的アウトカムに関与するメカニズムを明らかにするためにRNAシーケンス解析を行ったところ、血液凝固に関わるパスウェイやNET形成のパスウェイがクローン性造血を有するCTEPH患者で亢進していた。加えて、NETのマーカーである血清シトルリン化ヒストンH3がクローン性造血を有する患者で上昇していた。これらの結果は、血液疾患の既往がある患者を除外しても同様であった。
クローン性造血に関連した遺伝子変異を全体の20.1%のCTEPH患者で認めた。中でも年齢が80代の患者では、その割合は44.4%と非常に高かった。臨床的影響としては、クローン性造血を有するCTEPH患者では、治療1年後のBNPや在宅酸素療法使用率が高く、6分間歩行距離が短かった。また、クローン性造血を有する患者では、抗凝固療法を行っているにも関わらず、診断後肺動脈に新規血栓が出現するイベントの発生率が高く、さらには、治療完了後に病状が増悪し追加のBPA治療が必要となる頻度も高かった。これらの臨床的アウトカムに関与するメカニズムを明らかにするためにRNAシーケンス解析を行ったところ、血液凝固に関わるパスウェイやNET形成のパスウェイがクローン性造血を有するCTEPH患者で亢進していた。加えて、NETのマーカーである血清シトルリン化ヒストンH3がクローン性造血を有する患者で上昇していた。これらの結果は、血液疾患の既往がある患者を除外しても同様であった。
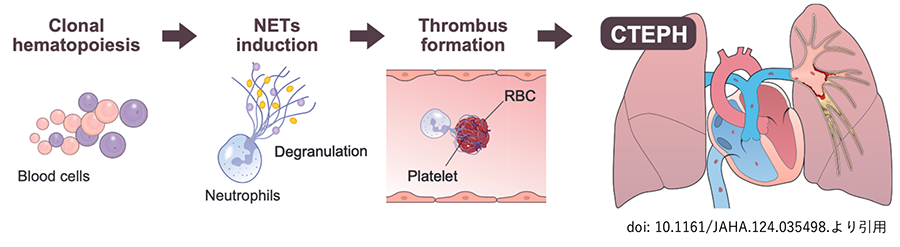
以上から、クローン性造血は好中球活性化やNET形成を介して血栓形成傾向を惹起し、CTEPHの病態生理やCTEPH患者における治療抵抗性と関連していることが示唆された。CTEPH患者においても遺伝学的検査によりクローン性造血の有無を評価することで、抗凝固療法やフォローアップの頻度を最適化することができると考えられた。本研究成果はJournal of the American Heart Association誌に掲載された(Momoi M, et al. J Am Heart Assoc. 2024;13:e035498.)。
②RNF213関連血管疾患としてのCTEPH
近年RNF213 p.R4810K変異は、もやもや病やPPSをはじめとした全身の血管疾患と関連した遺伝子変異として報告されているが、CTEPH患者におけるその頻度や臨床的影響は明らかではなかった。本研究では2009年から2021年にBPAを受けた、静脈血栓塞栓症の既知のリスク因子を持たないCTEPH患者140名を対象に、RNF213 p.R4810K変異の有無を評価した。
RNF213 p.R4810Kヘテロ接合性変異が、6.4%のCTEPH患者に認められ(アレル頻度:3.2%)、日本人一般集団でのアレル頻度(0.84%)に比べて有意に高かった。この変異を持つ患者は、診断時の年齢が若く(56歳 vs. 67歳, p=0.032)、平均肺動脈圧が有意に高かった(47mmHg vs. 38mmHg, p=0.035)。また、poor subpleural perfusion (PSP)が高頻度に認められ(66.7% vs. 9.2%, p<0.001)、BPA後の平均肺動脈圧および肺血管抵抗が変異を持たない患者よりも有意に高かった。BPAのセッション回数も多く(7.33回 vs. 5.18回, p=0.011)、この傾向は多変量解析でも確認された(p=0.016)。
これらの結果より、CTEPH患者の一部は、RNF213関連血管疾患としての表現型を呈している可能性が示された。遺伝学的検査によるCTEPH患者でのRNF213 p.R4810K変異の検出は、病態を理解し治療反応を予想する上で重要であると考えられた。本研究成果はJACC: Asia誌に掲載された(Momoi M, et al. JACC: Asia. 2024;4:1017–1019.)。
横川 哲朗(福島県立医科大学循環器内科学講座)
「肺高血圧症における右心不全バイオマーカー同定と病態の解明」
研究要旨
肺動脈性肺高血圧症では、右心不全が主要な死因の一つとなる。そのため、右心不全の評価や早期発見するための右心不全バイオマーカーの同定が期待されている。申請者は、心臓線維化に関わる重要な蛋白であるCollagen triple helix repeat containing protein 1(CTHRC1)の右心不全バイオマーカーとしての意義を、モノクロタリン誘発性右心不全動物モデルの右室組織と、ヒト肺高血圧症の血液を用いたEnzyme-linked immunosorbent assay(ELISA)法で調べた。結果、右心不全モデル動物の右室組織ではCTHRC1発現が亢進しており、免疫染色でCTHRC1は右室線維化領域に一致して発現していた。さらに、肺動脈性肺高血圧症患者(n = 46)、慢性血栓塞栓性肺高血圧症患者(n = 64)、とコントロール(n = 20)の血液を用いてCTHRC1濃度を測定したところ、肺高血圧症においてCTHRC1濃度が有意に上昇しており、さらに右心機能を示すTricuspid lateral annular peak systolic velocityやRight ventricular fractional area changeと有意に関連していた。さらに慢性血栓塞栓性肺高血圧症患者(n = 64)においては、バルーン肺動脈形成術により、右心機能の改善と共に、血中CTHRC1濃度が有意に減少した。以上の検討により、CTHRC1が肺高血圧症患者における新規右心不全バイオマーカーとなることを明らかにした。本研究成果は筆頭著者として報告した(Yokokawa T, et al. Can J Cardiol 40, 2281-2288, 2024)。
また申請者は、Proximity extension assay法(Inflammation Panel)による血漿プロテオミクス解析を用いて、血行動態が正常なコントロール(n = 28)、肺動脈性肺高血圧症患者(n = 60)由来の血液を解析した。検討された384種の蛋白の中で、51種の蛋白が肺高血圧症患者の血液において有意に上昇していた。さらに多変量解析では、CRIM1、HGF、FSTL3、PLAUR、CLSTN2、SPON1といった6種の蛋白が、死亡/肺移植イベントと独立して関連していた。肺高血圧症患者と肺高血圧症モデル動物由来の右心不全右室組織を用いた検討では、肺高血圧症の右心不全右室において、FSTL3とSPON1が有意に上昇していた。以上の検討により、FSTL3とSPON1が肺高血圧症患者において、右心不全に関連した血中予後予測バイオマーカーとなる可能性が示唆された。本研究成果は筆頭著者として報告した(Yokokawa T, et al. J Am Heart Assoc 13, e032888, 2024)。
さらに申請者は、肺高血圧症患者由来の右室組織(コントロール, n = 17; 代償期, n = 11; 非代償期, n = 11)と血漿(コントロール, n = 28; 肺動脈性肺高血圧症, n = 60)を用いたマルチオミックス解析を行った。患者由来の右室組織を用いたプロテオミクス解析で、非代償期の肺高血圧症の右室では、コントロールと比較し、LTBP2、COL6A3、COL18A1など92種の蛋白の発現が亢進していた。そして血漿を用いたProximity Extension Assay法(cardiometabolic proteins)による検討では、TGM2、NT-proBNPなど62種の蛋白が、コントロールと比較し、肺高血圧症患者で上昇していた。右室、血液いずれの解析においても有意に発現が亢進している蛋白の中で、血中濃度に代償期右心不全患者(心係数 2.2以上、n = 29)と非代償期右心不全患者(心係数 2.2未満、n = 31)での有意差があったのが、線維化に関連した蛋白であるLTBP2であった。その後行ったバイオマーカーとしての解析では、血中LTBP2濃度高値は、肺高血圧症患者の死亡/肺移植イベントと関連した。別の肺高血圧症患者コホート(n = 61)でも同様に血中LTBP2濃度は死亡/肺移植イベントと関連した。2つの肺高血圧症患者コホートを合わせたコホート(n = 121)を用いた多変量解析において、血中LTBP2濃度は肺動脈性肺高血圧症の予後不良と独立した関連があった。以上より血中LTBP2濃度は、肺高血圧症において、右心不全右室由来の予後予測バイオマーカーとなる可能性が示された。本研究成果は共著者として報告した(Boucherat O, Yokokawa T, et al. Nat Cardiovasc Res 1, 748 760, 2022)。
申請者は、動物実験により肺高血圧症の病態を明らかにするための研究も進めている。本態性血小板血症や骨髄線維症などの骨髄増殖性疾患に肺高血圧症が合併することは知られているが、その病態は不明であった。そのため、申請者は骨髄増殖性疾患に関連した遺伝子変異であるCalr変異に伴う肺高血圧症の発症メカニズムの検討を行った。病態解明のため、Calr変異を有する遺伝子改変マウスを作成。そしてCalr変異を有する遺伝子改変マウスの骨髄を移植したマウスでは、肺動脈周囲に骨髄由来マクロファージ集積が生じ、さらに肺組織でのエンドセリン1の発現上昇を介して、低酸素誘発性肺高血圧症が増悪することを明らかにした。本研究成果は申請者が共同筆頭著者として報告した(Minakawa K, Yokokawa T, et al. J Hematol Oncol 14, 52, 2021)。
吉田 賢明(九州大学病院循環器内科)
「肺動脈性肺高血圧症における三尖弁逆流量の病態意義の解明」
研究要旨
肺動脈性肺高血圧症において三尖弁逆流存在下での正確な右室機能評価の重要性
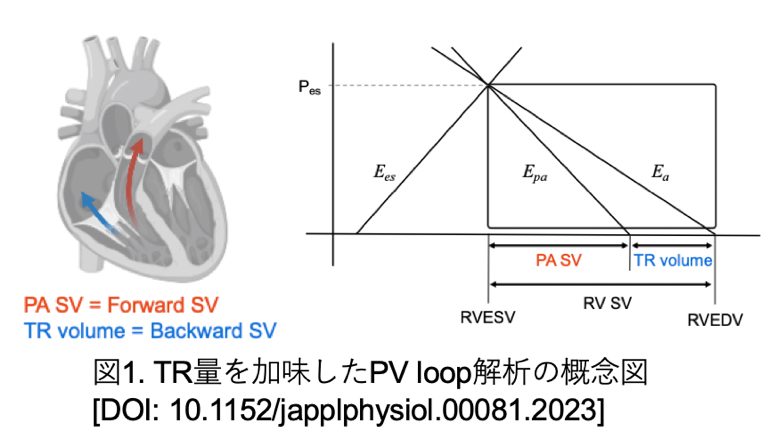 肺動脈性肺高血圧症(PAH)は肺血管抵抗(PVR)上昇に伴う右室(RV)機能障害から死に至る。上昇するPVRに対して循環を保つため、RVは代償して肥大し、収縮性を高める。RV代償は圧-容積曲線(PV loop)解析を用いてRVと肺動脈(PA)のcoupling(心収縮能指標/後負荷指標=Ees/Ea)が保たれていることで説明でき、病態進行によりRVが代償できなくなるとRV-PAのcoupling不全が認められるようになる(Vonk-Noordegraaf A, et al. J Am Coll Cardiol. 2017;69:236-243.)。一方で、病態が進行するとRVは拡大、収縮能は低下しtetheringによる機能性三尖弁閉鎖不全(TR)が出現するが(Gerçek M, et al. Front Cardiovasc Med. 2021;8:701243.)、従来のPV loop解析はTRが想定されていない。心室にとっての後負荷指標となる実行動脈エラスタンス(Ea)は収縮末期圧(Pes)を心室拍出量(SV)で除して得られるが、TRの存在下ではRV SVは順行性と逆行性に血液が駆出され、EaはRVにとって正味の後負荷は反映できるが順行性後負荷を反映できない。そこで、応募者は先行研究において、RV圧負荷モデルラットを用いてTRのPV loop解析への適応方法について検討を行い、新しいPV loop解析の概念を提唱した(図1, Yoshida K, et al. J Appl Physiol. 2023;135:53-59.)。
肺動脈性肺高血圧症(PAH)は肺血管抵抗(PVR)上昇に伴う右室(RV)機能障害から死に至る。上昇するPVRに対して循環を保つため、RVは代償して肥大し、収縮性を高める。RV代償は圧-容積曲線(PV loop)解析を用いてRVと肺動脈(PA)のcoupling(心収縮能指標/後負荷指標=Ees/Ea)が保たれていることで説明でき、病態進行によりRVが代償できなくなるとRV-PAのcoupling不全が認められるようになる(Vonk-Noordegraaf A, et al. J Am Coll Cardiol. 2017;69:236-243.)。一方で、病態が進行するとRVは拡大、収縮能は低下しtetheringによる機能性三尖弁閉鎖不全(TR)が出現するが(Gerçek M, et al. Front Cardiovasc Med. 2021;8:701243.)、従来のPV loop解析はTRが想定されていない。心室にとっての後負荷指標となる実行動脈エラスタンス(Ea)は収縮末期圧(Pes)を心室拍出量(SV)で除して得られるが、TRの存在下ではRV SVは順行性と逆行性に血液が駆出され、EaはRVにとって正味の後負荷は反映できるが順行性後負荷を反映できない。そこで、応募者は先行研究において、RV圧負荷モデルラットを用いてTRのPV loop解析への適応方法について検討を行い、新しいPV loop解析の概念を提唱した(図1, Yoshida K, et al. J Appl Physiol. 2023;135:53-59.)。
本研究は心臓磁気共鳴画像(CMR)を用いて、①PAH患者におけるTR量の病態意義を明らかにすること、②TRを加味したPV loop解析を行い、PAHにおける詳細なRV評価を行うこと、③血行動態シミュレーションを用いてTRに介入した際にRVへの影響を検討すること、を目的とした。
① 肺動脈性肺高血圧症患者における三尖弁逆流量評価の重要性
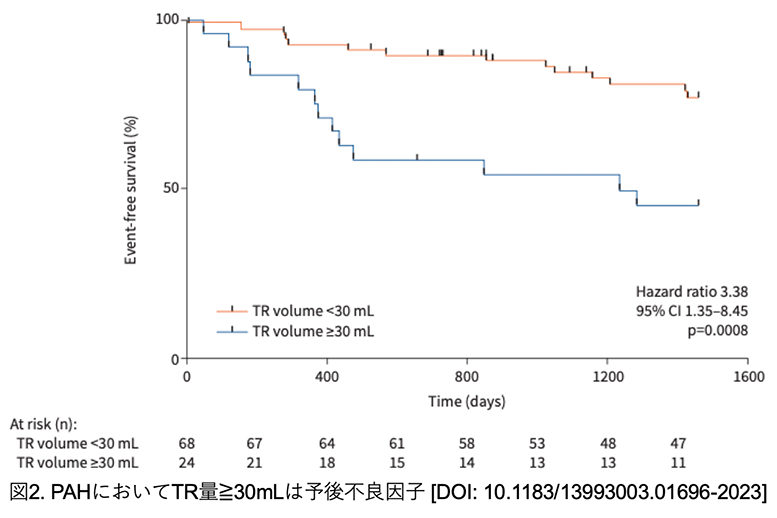 Amsterdam UMCにおいて2010年1月1日から2021年8月31日の間にPAHと診断された患者のCMRを用いて、TR量の定量評価を行った。TR量はRVとPAのSVの差から間接的に求めた。92名のCMRを用いて解析を行ったところ、TR量≧30 mLの患者は全体の26%を占めていた。TR量30mLをcutoffとすると、30mL未満の患者に対して30mL以上の患者ではevent-free survivalが不良であった(図2)。
Amsterdam UMCにおいて2010年1月1日から2021年8月31日の間にPAHと診断された患者のCMRを用いて、TR量の定量評価を行った。TR量はRVとPAのSVの差から間接的に求めた。92名のCMRを用いて解析を行ったところ、TR量≧30 mLの患者は全体の26%を占めていた。TR量30mLをcutoffとすると、30mL未満の患者に対して30mL以上の患者ではevent-free survivalが不良であった(図2)。
② 肺動脈性肺高血圧症患者における三尖弁逆流と右室機能評価
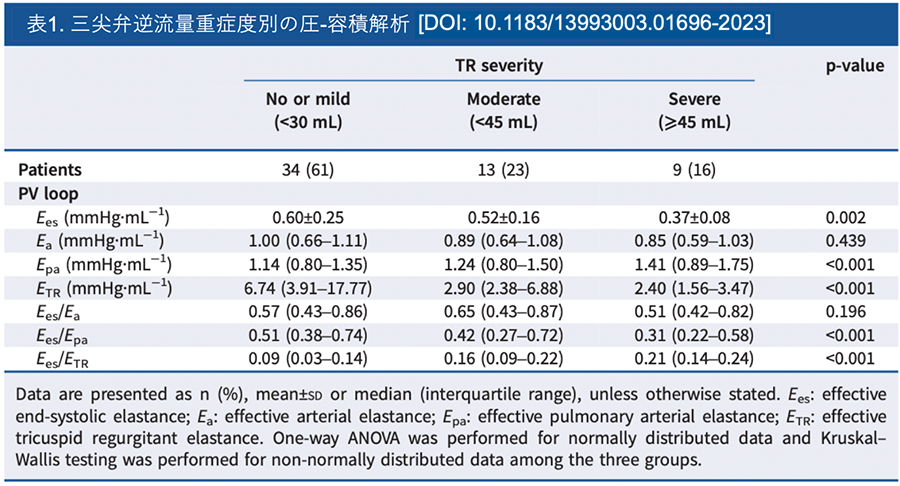
続いて、CMRによって得られた右室容積、TR量と、右心カテーテル検査より得られた圧データを用いてPV loop解析を行った。するとTR量が重症になるにつれ、RVEFには違いが見られなかったが、負荷非依存の収縮特性を表すEesは低下しており、またEpaは上昇しており、RV-PA couplingの指標であるEes/Epaは低下していることが明らかとなった。
③ 肺動脈性肺高血圧症性に対する三尖弁修復術の血行動態シミュレーション
PAHに対して三尖弁修復術を行った場合に想定されるRVへの影響を、オンライン血行動態シミュレーションソフトウェアであるHarvi (Doshi D, et al. J Card Fail. 2016;22:303-311.)を用いて検討した。
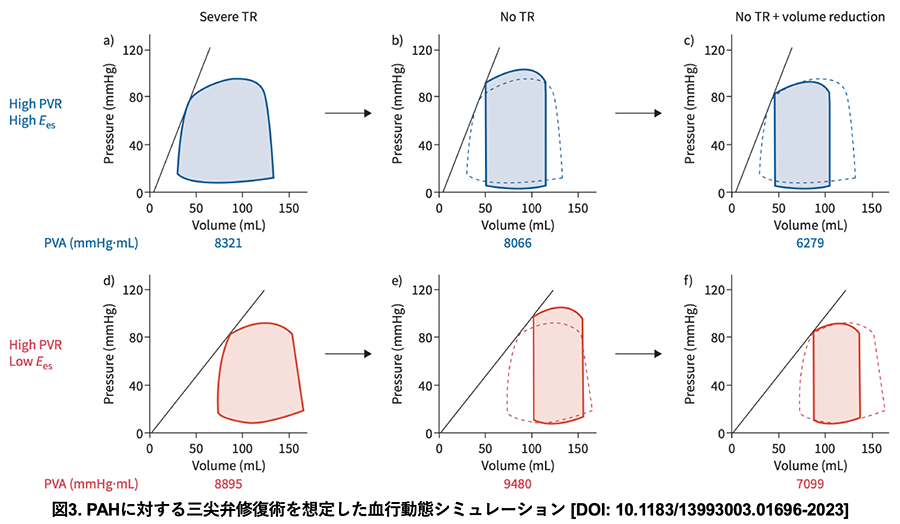
心筋酸素消費量の指標としてPV area (PVA)を用いた。Eesが高い場合(図3上)、TRが消失するとPVAは低下し、RV負荷なく血行動態改善が期待できる。一方Eesが低い場合(図3下)、TR消失によりPVAが増加し、RV機能破綻が危惧される可能性が示された。
以上よりPAH患者においてTR量は予後規定因子であること、TR量が増加するにつれRV収縮性の低下、RV-PA coupling不全と関連があること、シミュレーションから三尖弁修復術はEesが保たれた症例を見極める必要があることが明らかとなった。これらの結果を昨年European Respiratory Journalに投稿し(Yoshida K, et al. Eur Respir J. 2024;63:2301696.)、併せてEditorialも掲載された(Thenappan T. Eur Respir J. 2024;63:2400797.)。これらの業績が認められ、European Respiratory Society刊行予定のERS Monograph; Pulmonary Hypertension中のChapter 15: Tricuspid Regurgitation in Pulmonary Arterial Hypertensionの執筆を委任され、現在投稿中である。
